Vers une alternative plus durable de la transformation du méthane en hydrogène et hydrocarbures grâce à une transition de phase électronique dans le dioxyde de vanadium
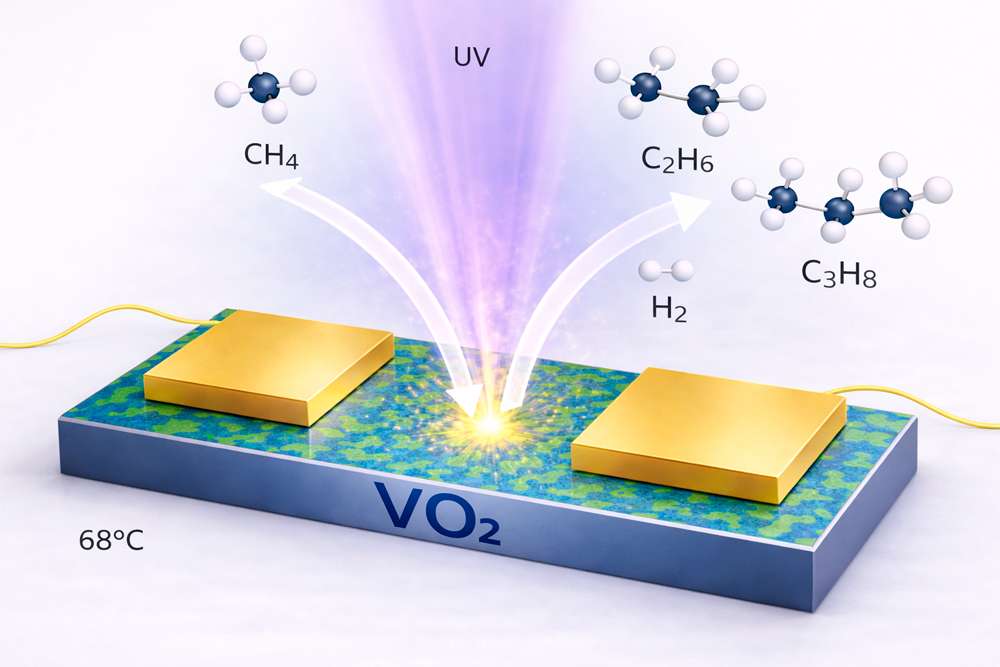
Optimiser l’efficacité des photocatalyseurs constitue un enjeu clé pour la conversion du méthane. Elle repose sur l’absorption lumineuse et le transport des charges photo-induites vers la surface des photocatalyseurs. Des chercheurs viennent de montrer que le dioxyde de vanadium VO₂, qui change d’état électronique à 68 °C, facilite considérablement le transfert de ces charges pour réagir avec le méthane lors de cette transition. Des films minces de VO₂ permettent ainsi une conversion photocatalytique record du méthane en dihydrogène, éthane et propane. En réduisant leur épaisseur, la réaction conduit à un seul hydrocarbure, le propane, offrant une méthode plus durable que les procédés industriels actuels.
Le méthane est un gaz très abondant mais difficile à transformer, car il réagit peu. Pour y parvenir, les chercheurs utilisent des photocatalyseurs, matériaux qui absorbent l’énergie lumineuse et l’exploitent ensuite pour produire une réaction chimique. Mais une grande partie de cette énergie se dissipe rapidement, ce qui rend inefficace l’activation du méthane à la surface des photocatalyseurs.
Une équipe de scientifiques(1) a montré qu’un composé, l’oxyde de vanadium VO₂, possède une propriété idéale pour contourner ce problème.
À 68 °C, le VO₂ change brutalement d’état : il passe d’isolant à métallique. Pendant cette transition, les deux états coexistent en s’entremêlant à l’échelle nanométrique. Les nombreuses frontières entre ces zones séparent efficacement les charges produites par la lumière. Celles-ci atteignent alors la surface du matériau en grand nombre, ce qui rend la réaction beaucoup plus efficace.
Grâce à cette transition, des minces films de VO₂ transforment le méthane en molécules utiles comme l’hydrogène, l’éthane ou le propane, avec, sous certaines conditions expérimentales, une production sélective d’un des deux hydrocarbures. La transition peut même être déclenchée électriquement à plus basse température, ouvrant la voie à des photocatalyseurs plus performants et moins énergivores.
(1) IEMN (Univ. Lille, CNRS, Centrale Lille, Univ. Polytechnique Hauts-de-France, Junia), UCCS (Univ. Lille, CNRS, Centrale Lille, ENSCL, Univ. Artois), UMET (CNRS, INRAE, Centrale Lille), LASIRE (Univ. Lille, CNRS), LPEM (ESPCI Paris, PSL Université, CNRS, Sorbonne Université), XLIM et IRCER (CNRS/ Université de Limoges).
En savoir +
Contact : bruno.grandidier![]() iemn.fr
iemn.fr
Double distinction pour le doctorant My Nghe Tran
Dans le cadre de ces recherches, le doctorant My Nghe Tran, encadré par Bruno Grandidier (IEMN) et Vitaly Ordomsky (UCC-CNRS), s’est distingué par des travaux innovants en photocatalyse, récompensés par le prix de la meilleure thèse de l’Université de Lille.
Le 4 décembre 2025, My Nghe Tran avait déjà eu l’honneur de recevoir le premier prix de thèse décerné par la Société chimique de France (SCF), section Hauts-de-France.
Ce prix récompense l’importance, l’originalité et les contributions innovantes de sa thèse de doctorat, qui portait sur l’amélioration de l’efficacité de la conversion d’énergie par photocatalyse à l’aide d’un champ électrique externe modéré.